Plasticidad cerebral: evaluación y usos clínicos en el daño cerebral adquirido
26/10/2021 Foto: Federación Española de Daño Cerebral.
Foto: Federación Española de Daño Cerebral.La plasticidad cerebral forma parte del día a día de todos los seres humanos y nos permite adaptarnos a nuestro entorno. La plasticidad se define como «la capacidad del sistema nervioso para cambiar su actividad en respuesta a estímulos intrínsecos o extrínsecos mediante la reorganización de su estructura, funciones o conexiones» (Mateos-Aparicio y Rodríguez-Moreno, 2019), y es fundamental para establecer y mantener conexiones cerebrales, adquirir nuevas habilidades y recuperarse o adaptarse después de una lesión cerebral, como un ictus o un traumatismo craneoencefálico (TCE). A pesar de que se suele hablar de plasticidad cuando alguien ha sufrido algún tipo de daño cerebral adquirido, la realidad es que esta capacidad está presente y activa a lo largo de toda nuestra vida.
La neuroplasticidad se puede manifestar de dos maneras: estructural y funcionalmente. La plasticidad estructural se produce cuando hay cambios físicos en el cerebro, por ejemplo, cuando se crean nuevas conexiones neuronales o se refuerzan las existentes. La plasticidad funcional está relacionada con la versatilidad del cerebro para conseguir que las neuronas de un área puedan realizar funciones de otra región. Esta capacidad es particularmente interesante en casos en que el cerebro ha sufrido algún tipo de daño cerebral adquirido, como un TCE (por ejemplo, accidente de tráfico o deportivo, una agresión, etc.) o un accidente cerebrovascular (ictus).
Las consecuencias de un TCE abarcan desde déficits cognitivos (en atención, memoria, flexibilidad cognitiva, planificación, razonamiento, etc.) hasta alteraciones en la emoción y la conducta (por ejemplo, falta de inhibición, problemas en las interacciones sociales, ansiedad, depresión, etc.). La recuperación de estos déficits depende en cierto modo de la plasticidad cerebral, la habilidad del cerebro de reorganizar su estructura, funciones o conexiones. Hay evidencias científicas que muestran alteraciones en la plasticidad cerebral después de un TCE, y cierta mejora en la plasticidad después de la rehabilitación cognitiva, pero se trata de evidencias escasas e insuficientes para poder extraer conclusiones. Por eso, es necesario profundizar en la patofisiología del TCE y establecer biomarcadores que ayuden a lograr pronósticos más precisos y a definir abordajes terapéuticos más eficaces.
En este sentido, la estimulación magnética transcraneal (transcranial magnetic stimulation, TMS) permite evaluar la plasticidad cerebral en humanos de forma segura y confortable y, combinada con otras técnicas neurofisiológicas, como por ejemplo el electromiograma (EMG), ofrece un poderoso enfoque para profundizar en la comprensión de la plasticidad cerebral, las bases neurofisiológicas de la disfunción cognitiva y las relaciones entre el cerebro, la cognición y la conducta.
La TMS es una técnica de estimulación cerebral no invasiva, segura e indolora, que permite modular la actividad cerebral, y aumentarla o disminuirla en un área específica del cerebro. La base de la TMS es el principio de inducción electromagnética, descubierto por Michael Faraday en 1831. Este principio expone que una corriente eléctrica fluyendo a través de una bobina de hilo conductor genera un campo magnético que, a su vez, induce una corriente eléctrica secundaria en cualquier conductor próximo. En el caso de la TMS, el aparato de estimulación produce una corriente eléctrica de alta intensidad, de muy breve duración y rápidamente cambiante que pasa por un hilo de cobre encapsulado dentro de la bobina de estimulación. Si esta corriente eléctrica tiene suficiente intensidad y duración, generará un campo magnético que penetrará en el cráneo y las meninges y, gracias a la fluctuación de este campo magnético y a la capacidad de conducción eléctrica del tejido cerebral, provocará una corriente eléctrica en el cerebro.
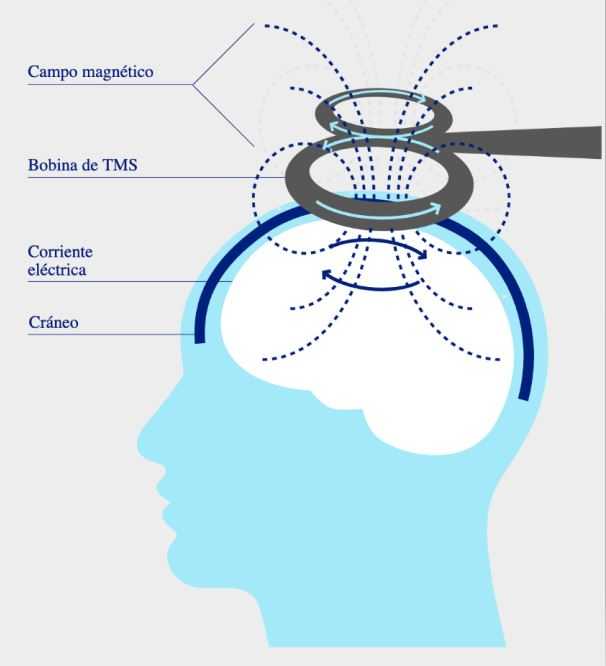
Por otro lado, el electromiograma es una técnica neurofisiológica que permite grabar la actividad eléctrica de los músculos con ayuda de unos electrodos que se posicionan sobre el músculo deseado.
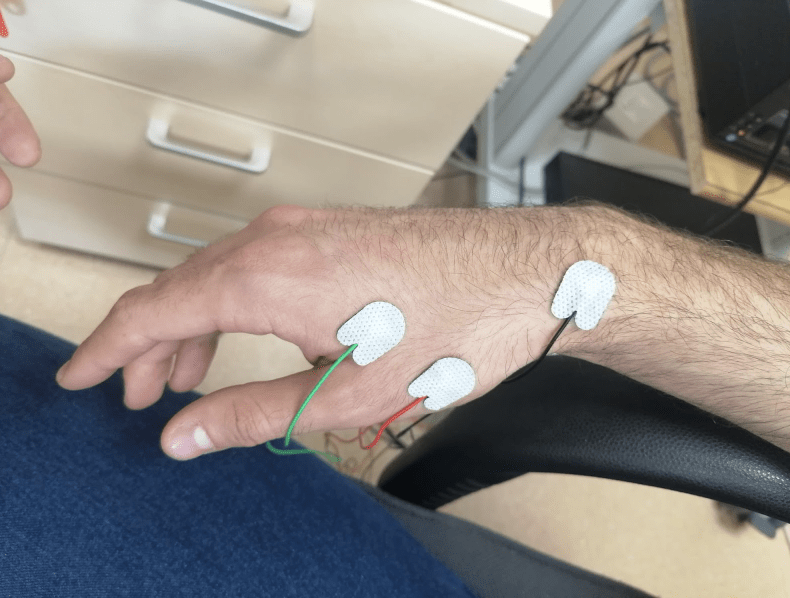
Para poder evaluar la plasticidad en este contexto, necesitamos obtener una medida objetiva: el potencial motor evocado (motor evoked potential, MEP). El MEP mide la actividad eléctrica de un músculo específico (primer interóseo dorsal) activado mediante la estimulación con TMS del área motora primaria del cerebro. Lo que interesa es conocer la amplitud del MEP, puesto que será la referencia a partir de la cual podremos conocer el grado de adaptabilidad del cerebro ante la modulación de su actividad neuronal mediante la TMS, es decir, su capacidad plástica.
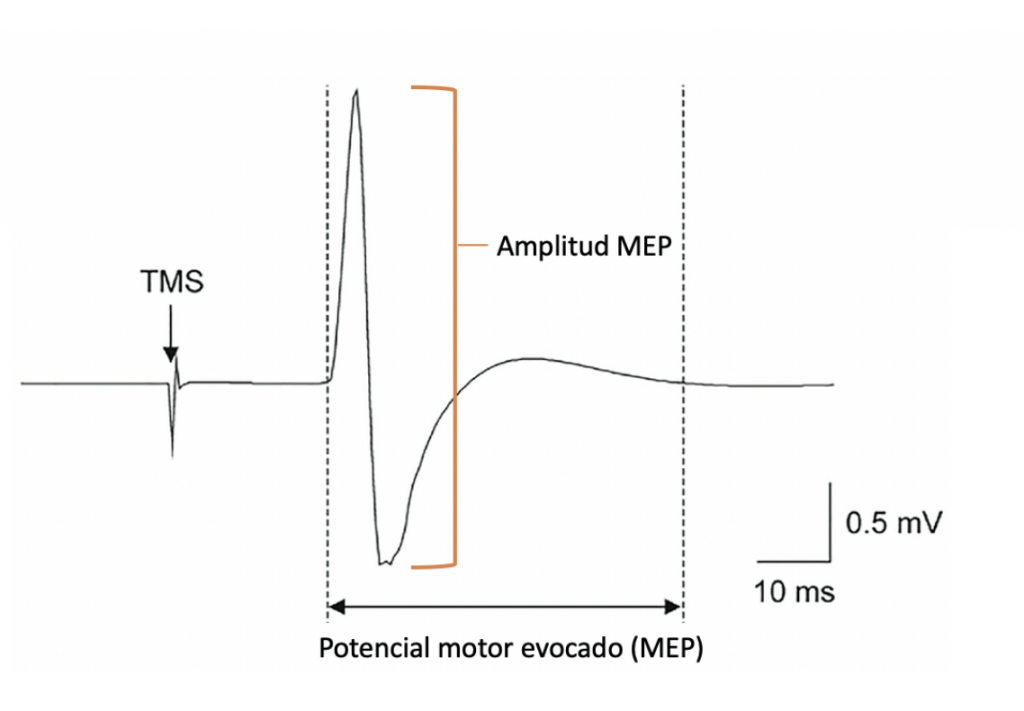
El primer paso del proceso es grabar 50 MEP y hacer el promedio para establecer así la línea base de referencia para cada persona. A continuación, se estimulará con TMS el área primaria motora para modular su activación. Hay varios protocolos de TMS que se pueden utilizar para ello, y dependiendo del que se emplee la excitabilidad cortical de esta región se verá incrementada o disminuida. Una vez aplicada la intervención, se grabarán de nuevo varios MEP, en diferentes momentos, durante los 30 minutos posteriores a la estimulación con TMS. El valor promedio que salga de cada grupo de MEP se comparará con el valor obtenido antes de la intervención (promedio de los 50 MEP iniciales), y así descubriremos si la persona presenta una plasticidad más o menos adaptativa. En otras palabras, se comparará la amplitud de los MEP previos a la TMS con la amplitud de los MEP posteriores. Si se ha aplicado un tipo de estimulación excitatoria, la amplitud de los MEP posteriores a la intervención deberá ser mayor que el valor de referencia, mientras que se espera que se produzca el efecto contrario en caso de haberse aplicado un protocolo inhibitorio. Si el cambio en las amplitudes de los potenciales no es lo bastante grande, consideraremos que la persona tiene la plasticidad alterada.
Obtener información sobre la integridad de la plasticidad cerebral nos permitirá conocer con mayor profundidad los mecanismos neurofisiopatológicos de los TCE y su evolución, y obtener un biomarcador que nos ayude en el diseño, selección e implementación de las intervenciones más adecuadas para cada persona en función de la patología, evolución y perfil de alteración.
Con esta elección personalizada del abordaje óptimo para cada persona conseguiremos mejores resultados de la intervención, tiempos de recuperación más cortos, y una mejora de la calidad de vida de las personas afectadas y sus cuidadores y familiares.
Referencias bibliográficas
Dilena, A., Todd, G., Berryman, C., Rio, E. y Stanton, T. R. What is the effect of bodily illusions on corticomotoneuronal excitability? A systematic review. PLoS ONE. 2019, 14(8), e0219754.
Mateos-Aparicio, P., Rodríguez-Moreno, A. The Impact of Studying Brain Plasticity. Front Cell Neurosci. 2019, 13:66.
Pascual-Leone, A., Amedi, A., Fregni, F. y Merabet, L. B. The Plastic Human Brain Cortex. Ann Rev Neurosci. 2005, 28:377.






Excelente texto! Muchas gracias.